principal de vitamina B12 es la síntesis por parte de las bacterias, hongos y algas. Los vegetales carecen de ella. Los requerimientos diarios mínimos son de 1-2 μg, el aporte diario normal (alimentos) es de 5-30 μg y el depósito corporal es de 2-4 mg, lo cual se requieren aproximadamente 1000 días para que se depleten los depósitos. Los niveles séricos normales son de 200-1.000 pg/ml.
Absorción y transporte. La vitamina B12 que procede de los alimentos, al llegar al estómago, se une a una proteína denominada proteína R o haptocorrina, de origen salival y gástrico. Este complejo pasa al duodeno, donde la vitamina B12 se escinde de la proteína R favorecido por las proteínas de la secreción pancreática, ya una vez libre la vitamina B12 se une al factor intrínseco de Castle (FI), que ha sido sintetizado por las células parietales de la mucosa gástrica (esta unión cobalamina-FI es favorecida por las proteasas pancreáticas y el pH alcalino del duodeno). El factor intrínseco es una glicoproteína termolábil, estable a pH alcalino, que se destruye fácilmente por las enzimas proteolíticas del estómago. Es una molécula dimérica que fija dos moléculas de vitamina B12, y su secreción es estimulada por la gastrina, histamina y la insulina. El complejo cobalamina-FI pasa al yeyuno y finalmente el íleon, donde se absorbe al unirse a un receptor específico en la mucosa denominado cubulina, ya una vez dentro del enterocito se separa de nuevo la cobalamina, que pasa a la sangre portal, donde es transportada por la transcobalamina II. Esta es la principal proteína de transporte de la vitamina B12 hacia los tejidos y el hígado (vesícula biliar) y su posterior ingreso a la circulación enterohepática.
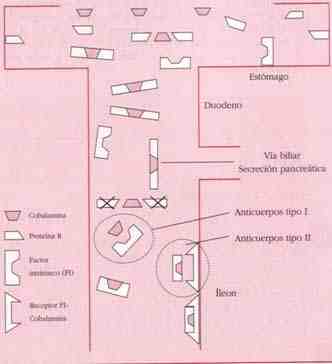
El recambio diario de la vitamina B12 refleja los requerimientos tisulares y su amplia reserva corporal (2-4 mg). De 1 a 10 μg de vitamina se deposita en el hígado (reservas hepáticas) en un adulto normal con una dieta adecuada. Se ha descrito la existencia de dos tipos de anticuerpos denominados: anticuerpos tipo I o bloqueadores (los más frecuentes y bloquean la unión cobalamina-FI), y anticuerpos tipo II, fijadores o precipitantes (bloquean la unión del complejo cobalamina-FI a la cubulina). Estos anticuerpos son altamente específicos en pacientes con anemia perniciosa (figura 2)
Figura 2. Absorción de la cobalamina
Se conocen cuatro formas de vitamina B12, que tienen en común un anillo corrínico + un átomo de Co2+ + un nucleótido y un grupo beta unido a la cobalamina, que puede ser de cuatro tipos: metilo, hidroxilo, cianuro, adenosilo que son los que diferencia una forma de otra. En vista de lo anterior existen cuatro formas: dos formas in vivo y dos formas farmacéuticas. In vivo: metilcobalamina (forma circulante) y adenosilcobalamina (forma de depósito). Farmacéuticas: hidroxicobalamina (uso terapéutico) y cianocobalamina (uso diagnóstico: prueba de Schilling).
Función. El déficit de vitamina B12 produce: 1. Una alteración en la síntesis de ADN y 2. Una degradación anormal de los ácidos grasos.
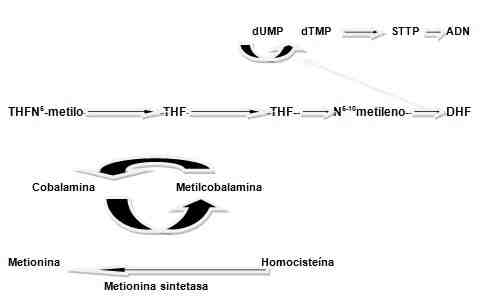
1. La vitamina B12 es necesaria para la síntesis de la metionina, participa en una reacción intermedia para la síntesis del ADN. Para esta reacción la vitamina B12 (cobalamina) sufre una metilación y se convierte en metilcobalamina. La metilcobalamina actúa como una coenzima en conjunto con la metionina sintetasa para convertir la homocisteína en metionina. La cobalamina acepta un grupo metilo del THF N(5) –metilo y lo transfiere a la homocisteína. Lo importante de esta reacción es que el THF se forma por la desmetilación del N(5) –THF. El THF se convierte luego en THF N(5-10) –metileno, forma necesaria para la síntesis del timidilato. Un déficit de cobalamina significa que el folato queda atrapado en la forma de THF N(5) metilo. Esto se conoce como la “trampa del folato”, por lo tanto el déficit de cobalamina conduce a aún déficit funcional de la actividad del ácido fólico para la síntesis de ADN (figura 3).
Figura 3. Reacciones bioquímicas que utilizan la cobalamina.
2. La vitamina B12 también interviene en una etapa del catabolismo del propionato, la isomerilización de la metilcobalamina-CoA a Succinil-CoA (Figura 4)
Figura 4. Reacciones bioquímicas que utilizan la cobalamina
Adenosilcobalamina
Propionil-CoA —> Metilmalonil-CoA —> Succinil-CoA
La desmielinización de las fibras nerviosas deriva de un defecto en la degradación del propionil-CoA a metilmalonil-CoA y por último a succinil-CoA. Conforme propionil-CoA se acumula, las células lo utilizan para la síntesis de ácidos grasos, supliendo al acetil-CoA habitual. De este modo se sintetizan ácidos grasos con un número impar de carbonos, los cuales se incorporan en las membranas neuronales alterando sus funciones, ocasionado la respectiva desmielinización y por ende las alteraciones neurológicas pertinentes.
En conclusión la vitamina B12 interviene en dos reacciones enzimáticas: 1. Citoplasmática. Metilación del ácido fólico (metilcobalamina) y, 2. Mitocondrial. Síntesis metilmalonil- CoA (adenosilcobalamina) a succinil-CoA.
Absorción y distribución del ácido fólico
La mayor parte de los alimentos contienen ácido fólico, entre ellos, la leche, los huevos, la levadura y el hígado, pero predomina en los vegetales de hojas verdes de donde toma su nombre. También es sintetizado por los microrganismos. Es termolábil, de allí que cuando los alimentos se cocinan en exceso se destruye gran parte del folato. El ácido ascórbico protege a los folatos de la oxidación. Los requerimientos diarios mínimos son de 50-100 μg, el aporte diario en la dieta normal es de 500-1000 μg, con unos depósitos